| Saúde |
Novo estudo comprova que a COVID-19 grave é uma doença trombótica
A trombose em pequenos vasos (capilares) do pulmão é uma das primeiras consequências da COVID-19 grave, precedendo até mesmo a dificuldade respiratória decorrente do chamado dano alveolar difuso.
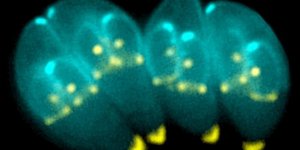
Pesquisadores da USP analisaram tecidos de nove pacientes que morreram de COVID-19. Ilustração: Elia Caldini
A partir da autópsia de nove pacientes que morreram após desenvolver a forma grave da doença, foi possível observar um quadro muito característico, envolvendo alterações na vascularização pulmonar e trombose.
No trabalho, os pesquisadores descrevem, pela primeira vez, aspectos relacionados ao dano endotelial e à formação de trombos ocasionados pela infecção. As descobertas – entre elas a constatação de que a COVID-19 tem como caráter central a formação de trombos na microcirculação pulmonar – contribuem para o entendimento da fisiopatologia da enfermidade e o desenvolvimento de novas estratégias terapêuticas.
“Esse estudo foi a prova final do que vínhamos alertando desde o comecinho da pandemia: a COVID-19 grave é uma doença trombótica. O vírus SARS-CoV-2 tem um tropismo pelo endotélio [é atraído para esse tecido], a camada de células que reveste os vasos sanguíneos. Portanto, ao invadir as células endoteliais, ele afeta primeiro a microcirculação. O problema começa nos capilares do pulmão, para depois ir coagulando os vasos maiores, podendo atingir qualquer outro órgão”, explica a pneumologista Elnara Negri, professora da Faculdade de Medicina da Universidade de São Paulo (FM-USP), coautora do artigo e uma das primeiras pesquisadoras do mundo a trabalhar com essa hipótese.
No estudo, apoiado pela FAPESP, os autores observaram por microscopia eletrônica o efeito do vírus nas células endoteliais do pulmão de pacientes que morreram com COVID-19 grave no Hospital das Clínicas (HC) da FM-USP.
A partir de autópsia minimamente invasiva, foi possível observar em todas as amostras a alta prevalência de microangiopatia trombótica – oclusão generalizada na microcirculação por trombose.
As amostras analisadas são oriundas de pacientes que foram hospitalizados entre março e maio de 2020.
Todos os pacientes foram intubados, necessitaram de terapia intensiva e morreram de hipóxia refratária (insuficiência respiratória). Vale destacar que nenhum paciente incluído no estudo foi tratado com anticoagulantes, pois essa não era a diretriz para o tratamento de COVID-19 naquele momento.
Também não existiam vacinas disponíveis na época.
Negri explica que, revestindo o endotélio, existe uma camada glicoproteica denominada glicocálix, que faz com que o sangue passe naturalmente pelas artérias, veias e capilares sem coagular.
“Alguns estudos anteriores realizados por Helena Nader na Unifesp [Universidade Federal de São Paulo] mostraram que, para invadir a célula, o vírus se liga principalmente ao receptor ACE-2 [proteína encontrada na superfície de diversas células do corpo, inclusive nas do epitélio e endotélio do sistema respiratório]. No entanto, antes disso, ele se liga ao heparan sulfato [um polissacarídeo] associado à membrana das células endoteliais, que forma justamente o glicocálix. Portanto, quando o SARS-CoV-2 invade o endotélio, ele o descama e destrói o glicocálix. Isso resulta em exposição tecidual e na coagulação intravascular, começando na microcirculação”, detalha Negri.
Como a ação inicial do vírus é na microcirculação pulmonar, os exames contrastados para investigação de presença de trombos em vasos maiores, realizados em pacientes com COVID-19 grave na época, nunca detectaram o problema precocemente.
No entanto, explica Negri, a disfunção endotelial é um fenômeno-chave na COVID-19, pois está diretamente associada à ativação da resposta inflamatória característica da doença.
“A invasão massiva do vírus e a destruição do endotélio promovem a ruptura da barreira endotelial e o recrutamento de células imunes circulantes, ativando vias relacionadas à trombogênese e à inflamação”, diz.
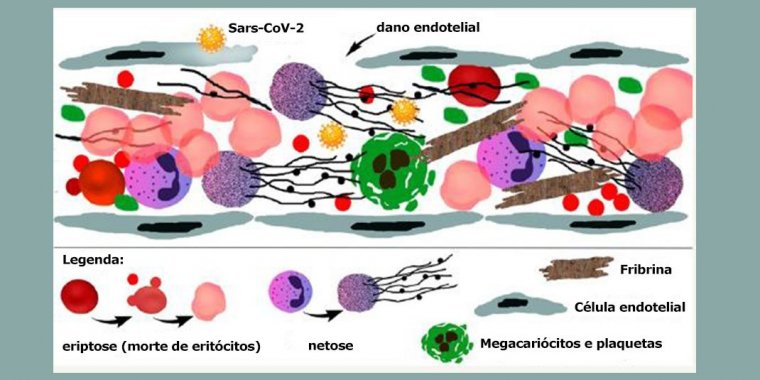
No trabalho, os pesquisadores observaram que o dano causado no endotélio tende a preceder duas características comuns a casos de desconforto respiratório: o vazamento significativo da membrana alvéolo-capilar dos pulmões e o acúmulo de polímeros de fibrina (proteína associada à coagulação e ao processo de cicatrização) nos alvéolos pulmonares.
Um trabalho do mesmo grupo da FM-USP, liderado por Thais Mauad, incluindo análise do transcriptoma (conjunto de moléculas de RNA expressas em um tecido), demonstrou que diversas vias associadas à coagulação, à ativação de plaquetas e à formação de trombos já estavam ativadas precocemente nos pulmões de pacientes com dano alveolar, precedendo a inflamação.
A análise confirmou ainda que não se trata de uma coagulação comum, desencadeada pela ativação dos fatores de coagulação.
“Na COVID-19, a coagulação se dá por lesão endotelial e é potencializada por netose [mecanismo imune que consiste na saída do material genético contido no núcleo dos neutrófilos em forma de redes – as NETs – na tentativa de prender e matar o patógeno] e pela lesão das hemácias com dimorfismo [uma alteração morfológica das células vermelhas do sangue] e ativação plaquetária. Portanto, existe toda uma estrutura para que o sangue fique mais denso e provoque tantas complicações”, afirma.
A pesquisadora ressalta ainda que, nesse cenário, onde o sangue se torna muito viscoso e altamente trombogênico, o paciente precisa ser mantido hidratado, diferentemente do que é preconizado para o tratamento do dano alveolar difuso. “Além disso, o timing e o controle rigoroso da anticoagulação são fundamentais”, alerta.
Não por acaso, outro estudo do mesmo grupo, com a participação das pesquisadoras Marisa Dolhnikoff e Elia Caldini, demonstrou que o dano pulmonar em casos graves de COVID-19 está associado ao nível de netose.
Ao analisar amostras de tecido de autópsia pulmonar, os cientistas observaram que, quanto mais elevado era o nível de NETs, maior era o dano pulmonar dos pacientes.
“O segredo para tratar o paciente com COVID-19 grave é mantê-lo hidratado e usar anticoagulante na dose certa, checando o nível adequado de anticoagulação em ambiente hospitalar assim que ele começa a dessaturar, ou seja, ter baixa de oxigênio no sangue. Depois disso, é preciso manter controle diário dos níveis terapêuticos de anticoagulação por meio de exames de sangue, sempre em ambiente hospitalar para não haver risco de sangramento, e a profilaxia de quatro a seis semanas em média após a alta, que é o tempo de o endotélio se refazer”, comenta.
A pesquisadora explica que esse protocolo com hidratação e o uso de anticoagulantes se dá porque, diferentemente das outras síndromes agudas respiratórias (SARS), nas quais o problema da falta de passagem de oxigênio dos pulmões para o sangue está principalmente relacionado com a inflamação nos alvéolos pulmonares, na COVID-19 grave inicial o dano endotelial dos capilares pulmonares é predominante. (Maria Fernanda Ziegler/Agência FAPESP)
VOCÊ TAMBÉM PODE ESTAR INTERESSADO EM